Hal ini dapat berupa proses redoks yang sederhana seperti oksidasi karbon yang menghasilkan karbon dioksida, atau reduksi karbon oleh hidrogen menghasilkan metana(CH4), ataupun ia dapat berupa proses yang kompleks seperti oksidasi gula pada tubuh manusia melalui rentetan transfer elektron yang rumit.
Istilah redoks berasal dari dua konsep, yaitu reduksi dan oksidasi. Ia dapat dijelaskan dengan mudah sebagai berikut:
- Oksidasi menjelaskan pelepasan elektron oleh sebuah molekul, atom, atau ion
- Reduksi menjelaskan penambahan elektron oleh sebuah molekul, atom, atau ion.
Reaksi non-redoks yang tidak melibatkan perubahan muatan formal (formal charge) dikenal sebagai reaksi metatesis.
Oksidator dan reduktor
Senyawa-senyawa yang memiliki kemampuan untuk mengoksidasi senyawa lain dikatakan sebagai oksidatif dan dikenal sebagai reduktor atau agen oksidasi. Oksidator melepaskan elektron dari senyawa lain, sehingga dirinya sendiri tereduksi. Oleh karena ia "menerima" elektron, ia juga disebut sebagai penerima elektron. Oksidator bisanya adalah senyawa-senyawa yang memiliki unsur-unsur dengan bilangan oksidasi yang tinggi (seperti H2O2, MnO4−, CrO3, Cr2O72−, OsO4) atau senyawa-senyawa yang sangat elektronegatif, sehingga dapat mendapatkan satu atau dua elektron yang lebih dengan mengoksidasi sebuah senyawa (misalnya oksigen, fluorin, klorin, dan bromin).Senyawa-senyawa yang memiliki kemampuan untuk mereduksi senyawa lain dikatakan sebagai reduktif dan dikenal sebagai [[oksidator ]] atau agen reduksi. Reduktor melepaskan elektronnya ke senyawa lain, sehingga ia sendiri teroksidasi. Oleh karena ia "mendonorkan" elektronnya, ia juga disebut sebagai penderma elektron. Senyawa-senyawa yang berupa reduktor sangat bervariasi. Unsur-unsur logam seperti Li, Na, Mg, Fe, Zn, dan Al dapat digunakan sebagai reduktor. Logam-logam ini akan memberikan elektronnya dengan mudah. Reduktor jenus lainnya adalah reagen transfer hidrida, misalnya NaBH4 dan LiAlH4), reagen-reagen ini digunakan dengan luas dalam kimia organik, terutama dalam reduksi senyawa-senyawa karbonil menjadi alkohol. Metode reduksi lainnya yang juga berguna melibatkan gas hidrogen (H2) dengan katalis paladium, platinum, atau nikel, Reduksi katalitik ini utamanya digunakan pada reduksi ikatan rangkap dua ata tiga karbon-karbon.
Cara yang mudah untuk melihat proses redoks adalah, reduktor mentransfer elektronnya ke oksidator. Sehingga dalam reaksi, reduktor melepaskan elektron dan teroksidasi, dan oksidator mendapatkan elektron dan tereduksi. Pasangan oksidator dan reduktor yang terlibat dalam sebuah reaksi disebut sebagai pasangan redoks.
Contoh reaksi redoks
Salah satu contoh reaksi redoks adalah antara hidrogen dan fluorin:Unsur-unsur, bahkan dalam bentuk molekul, sering kali memiliki bilangan oksidasi nol. Pada reaksi di atas, hidrogen teroksidasi dari bilangan oksidasi 0 menjadi +1, sedangkan fluorin tereduksi dari bilangan oksidasi 0 menjadi -1.
Ketika reaksi oksidasi dan reduksi digabungkan, elektron-elektron yang terlibat akan saling mengurangi:
Reaksi penggantian
Redoks terjadi pada reaksi penggantian tunggal atau reaksi substitusi.Sebagai contoh, reaksi antara larutan besi dan tembaga(II) sulfat:
Contoh-contoh lainnya
- Besi(II) teroksidasi menjadi besi(III)
- hidrogen peroksida tereduksi menjadi hidroksida dengan keberadaan sebuah asam:
- H2O2 + 2 e− → 2 OH−
- 2Fe2+ + H2O2 + 2H+ → 2Fe3+ + 2H2O
- denitrifikasi, nitrat tereduksi menjadi nitrogen dengan keberadaan asam:
- 2NO3− + 10e− + 12 H+ → N2 + 6H2O
- Besi akan teroksidasi menjadi besi(III) oksida dan oksigen akan tereduksi membentuk besi(III) oksida (umumnya dikenal sebagai perkaratan):
- 4Fe + 3O2 → 2 Fe2O3
- Pembakaran hidrokarbon, contohnya pada mesin pembakaran dalam, menghasilkan air, karbon dioksida, sebagian kecil karbon monoksida, dan energi panas. Oksidasi penuh bahan-bahan yang mengandung karbon akan menghasilkan karbon dioksida.
- Dalam kimia organik, oksidasi seselangkah (stepwise oxidation) hidrokarbon menghasilkan air, dan berturut-turut alkohol, aldehida atau keton, asam karboksilat, dan kemudian peroksida.
Reaksi redoks dalam industri
Proses utama pereduksi bijih logam untuk menghasilkan logam didiskusikan dalam artikel peleburan.Oksidasi digunakan dalam berbagai industri seperti pada produksi produk-produk pembersih.
Reaksi redoks juga merupakan dasar dari sel elektrokimia.
Reaksi redoks dalam biologi
 |
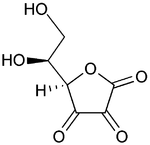 |
Atas: asam askorbat (bentuk tereduksi Vitamin C)
Bawah: asam dehidroaskorbat (bentuk teroksidasi Vitamin C)
Bawah: asam dehidroaskorbat (bentuk teroksidasi Vitamin C)
Pernapasan sel, contohnya, adalah oksidasi glukosa (C6H12O6) menjadi CO2 dan reduksi oksigen menjadi air. Persamaan ringkas dari pernapasan sel adalah:
- C6H12O6 + 6 O2 → 6 CO2 + 6 H2O
- Proses pernapasan sel juga sangat bergantung pada reduksi NAD+ menjadi NADH dan reaksi baliknya (oksidasi NADH menjadu NAD+). Fotosintesis secara esensial merupakan kebalikan dari reaksi redoks pada pernapasan sel:
- 6 CO2 + 6 H2O + light energy → C6H12O6 + 6 O2
Istilah keadaan redoks juga sering digunakan untuk menjelaskan keseimbangan antara NAD+/NADH dengan NADP+/NADPH dalam sistem biologi seperti pada sel dan organ. Keadaan redoksi direfleksikan pada keseimbangan beberapa set metabolit (misalnya laktat dan piruvat, beta-hidroksibutirat dan asetoasetat) yang antarubahannya sangat bergantung pada rasio ini. Keadaan redoks yang tidak normal akan berakibat buruk, seperti hipoksia, guncangan (shock), dan sepsis.
Siklus redoks
Berbagai macam senyawa aromatik direduksi oleh enzim untuk membentuk senyawa radikal bebas. Secara umum, penderma elektronnya adalah berbagai jenis flavoenzim dan koenzim-koenzimnya. Seketika terbentuk, radikal-radikal bebas anion ini akan mereduksi oskigen menjadi superoksida. Reaksi bersihnya adalah oksidasi koenzim flavoenzim dan reduksi oksigen menjadi superoksida. Tingkah laku katalitik ini dijelaskan sebagai siklus redoks.Contoh molekul-molekul yang menginduksi siklus redoks adalah herbisida parakuat, dan viologen dan kuinon lainnya seperti menadion.



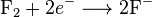

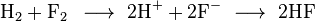







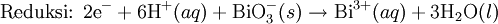










Tidak ada komentar:
Posting Komentar