Selain dari
ikatannya, terdapat cara lain untuk mengelompokan senyawa yakni
didasarkan pada daya hantar listrik. Jika suatu senyawa dilarutkan dalam
air dapat menghantarkan arus listrik disebut larutan elektrolit, dan sebaliknya jika larutan tersebut tidak dapat menghantarkan arus listrik disebut larutan nonelektrolit.
Glukosa (C6H12O6), etanol (C2H5OH), gula tebu (C12H22O11), larutan urea (CO(NH2)2) merupakan beberapa contoh senyawa yang dalam bentuk padatan, lelehan maupun larutan tidak dapat menghantarkan arus listrik.
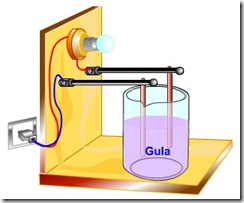
Cara pengujian
suatu senyawa termasuk elektrolit atau nonelektrolit dapat dilakukan
dengan meghubungkan baterai dan lampu bohlam atau amperemeter kemudian
ujung kabel dihubungkan pada dua buah elektroda. Satu sebagai anoda (+),
satu sebagai katoda (-).
Setelah semua
terhubung pengujian dapat dilakukan dengan mencelupkan kedua elektroda
ke dalam larutan yang akan diuji dan perhatikan agar kedua elektrode
tidak bersentuhan.
Ketika elektroda dicelupkan, jika lampu bohlam menyala dan atau
terbentuk gelembung udara pada kedua elektroda maka senyawa atau zat
tersebut termasuk golongan senyawa elektrolit.
Begitu pula
sebaliknya, ketika elektroda dicelupkan lampu bohlam tidak menyala dan
atau tidak terbentuk gelembung udara pada kedua elektroda, maka senyawa
atau zat tersebut termasuk golongan senyawa nonelektrolit.
Gambar Rangkaian Alat pengujian larutan